Què és l’acidificació de l’oceà? (problemàtica 1)
Els mars i els oceans representen al voltant del 71% de la superfície del planeta ocupen un volum de 1.400 milions de km3 i contenen més del 95% de l’aigua de tot el planeta.
Per tant, si mirem la Terra des de l’espai no pot passar desapercebuda la importància que les aigües oceàniques exerceixen sobre el nostre planeta, i és per això que s’anomena sovint planeta blau. Però li estem donant a la suficient importància? Tenim present quines són les seves problemàtiques ambientals?
Per donar resposta a aquestes preguntes volem tractar totes les problemàtiques actuals que pateixen els oceans. En aquesta primera entrada ens centrarem en l’acidificació dels oceans.
Augment del CO2
Segons el butlletí núm. 10 de la World Meteorological Organization sobre els gasos d’efecte hivernacle, la concentració del diòxid de carboni (CO2) ha augmentat un 42% des de l’inici de la revolució industrial (aproximadament l’any 1750) degut a les emissions de les cremes de combustibles fòssils, la producció de ciment i el canvi d’ús del sòl.
La continuada crema de combustibles fòssils augmenta els nivells de diòxid de carboni a l’atmosfera, que recau finalment als oceans. Els oceans actuen com a emmagatzematge e carboni, reduint els impactes associats al canvi climàtic terrestre. Si els oceans no juguessin aquest paper, la concentració de diòxid de carboni a l’atmosfera seria un 55% superior a la dels últims 250 anys.
Els oceans han absorbit grans quantitats de CO2 des dels inicis de la revolució industrial fins l’actualitat. Aquesta absorció és la causant del procés d’acidificació.
Què és l’acidificació de l’oceà?
El concepte acidificació es refereix al procés pel qual els oceans es tornen més àcids.
El CO2 absorbit per l’atmosfera reacciona amb l’aigua del mar formant àcid carbònic (H2CO3). Aquest àcid allibera un ió bicarbonat (HCO3-1) i un ió d’hidrogen (H+). L’augment dels ions d’hidrogen en el medi fa disminuir el pH. El pH és el coeficient que indica el grau de l’acidesa o alcalinitat d’una solució aquosa (pH= -log
En conclusió, el fet que hi hagi més ions d’hidrogen fa que l’oceà sigui més àcid, per tant, que el pH disminueixi.
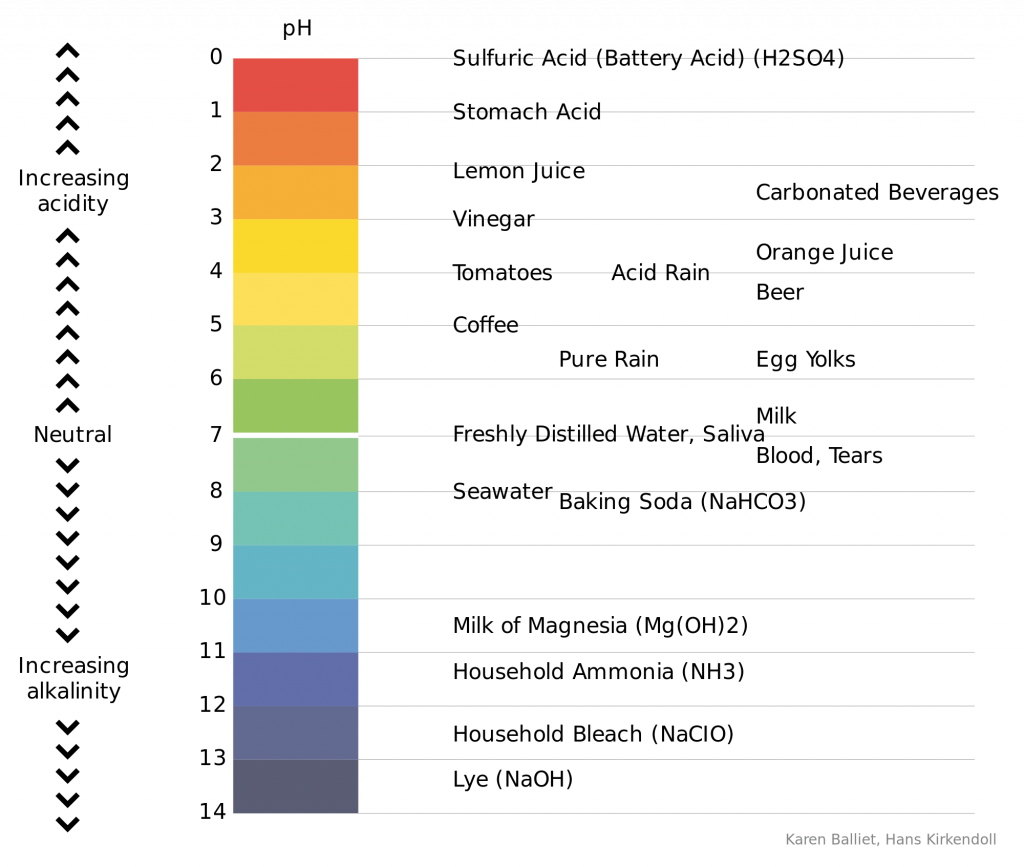
Imatge 1. autors Hans Kirkendoll i Karen Balliet
El pH de la superfície de l’oceà ha disminuït des de 8,2 a 8,1, que correspon amb un augment del 26% de H+. Mentre continuï augmentat el CO2 atmosfèric, cada vegada entrarà més a l’oceà, fent-lo més àcid i així reduint el pH.
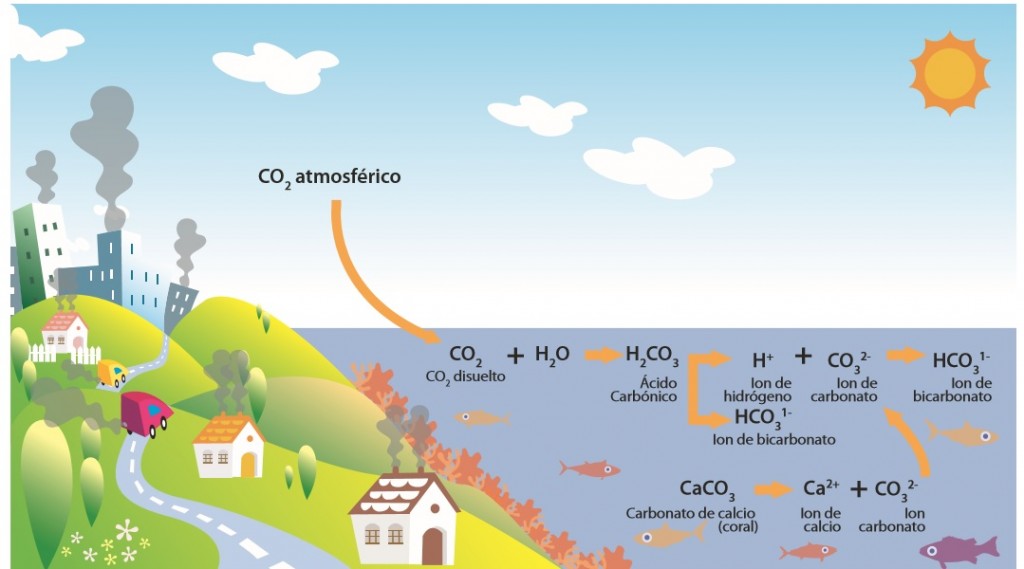
Imatge 2. extreta de la segona referència (2)
Efectes de l’acidificació dels oceans
Els processos biològics i fisiològics de molts organismes es veuen afectats per l’augment de l’acidesa, el que provoca grans canvis en molts organismes marins. Segons un informe de The Royal Society sobre l’acidificació de l’oceà, els efectes dels ecosistemes son molt greus i duradors.
Els organismes calcificadors es troben tant en ecosistemes d’aigües profundes com en aigües poc profundes. La calcificació és el procés fisiològic pel qual els organismes creen estructures com les closques i esquelets a partir del carbonat càlcic. Entre els organismes calcificadors es troben algunes de les espècies més abundants dels oceans, com els coralls, les cloïsses, el pteròpods, i altres mol·luscs, també crustacis com les llagostes i els crancs, i equinoderms com l’estrella de mar i alguns tipus de fitoplàncton.
Aquests organismes creen les seves estructures de carbonat càlcic a partir dels ions de calci (Ca2+) i carbonat (CO32-) existents a l’aigua que els rodeja. Els ions de calci abunden a l’oceà, però l’augment del CO2 a l’oceà, pot reduir aquests ions carbonats, fet que ralenteix o arribaria a parar la calcificació.
L’ió d’hidrogen que hem vist abans que s’alliberava de l’àcid carbònic, s’uneix als ions carbonats lliures a l’aigua i forma ions bicarbonat (HCO3-1). D’aquesta forma, el fet que hi hagi majors concentracions d’ió H+, fa disminuir la concentració d’ions carbonats (CO32-) disponibles pels organismes calcificadors.
L’acidificació dels mars i oceans, a més de disminuir la capacitat dels organismes calcificadors, també afecta a altres processos biològics i fisiològics. Aquests impactes poden incloure descensos en la taxa de creixement, ja que les fases larvària i juvenil són més sensibles a un augment de l’acidesa. Per exemple, la taxa de fecundació d’ous de dos espècies d’eriçó de mar (Hemicentrotus pucherrimus i Echirometra mathaei) ha disminuït davant d’una major acidificació.
Funcions fisiològiques vitals, com la respiració i els sistema nerviós també poden veure’s afectades, ja que l’acidificació pot provocar variacions en els nivells d’oxigen. Una conseqüència recau en els calamars, perquè degut a la seva intensa i energètica forma de nedar necessiten grans quantitats d’oxigen, el que els fa ser especialment sensibles a la seva absència.
Solucions
No existeixen unes solucions ràpides per aquesta problemàtica, tot i que el més eficaç i el que donaria bons resultats a llarg termini seria canviar de model energètic. Optar per eficiència energètica alternativa i sostenible, a més de reduir l’ús dels combustibles fòssils seria un gran avenç per poder reduir les emissions de carboni.
De la mateixa manera, una de les principals solucions seria adoptar polítiques d’estabilització del nivell del diòxid de carboni a l’atmosfera.
Amb tot plegat, la població té un paper més o menys important, i ara que tots som conscients de la problemàtica que ocasiona el diòxid de carboni als oceans, caldria preguntar-nos: com podem ajudar?
Referències
- VVAA (2015): Vigilancia del carbono oceánico y de la acidificación de los océanos. Boletín de la WMO 64 (1)
- IGBP, COI, SCOR (2013): La acidificación del océano. Resumen para responsables de políticas – Tercer simposio “El océano en un mundo con altos niveles de CO2. Programa Internacional Geosfera – Biosfera, Estocolmo (Suecia)
- HARROULD-KOLIEB, E; SAVITZ, J. (2009): Acidificación: ¿Cómo afecta el CO2 a los océanos? Oceana
- FABRY, VICTORIA J. (2008): Impacts of Ocean Acidification on Marine Fauna and Ecosystem Processes. ICES Journal of Marine Science, 65:414-432


